-
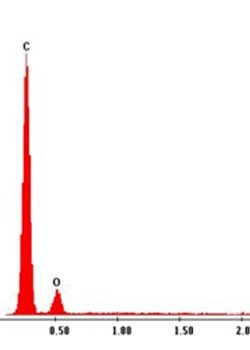
分析方法学验证技巧与重点
摘要:对于药学领域的方法验证ICH、药典委员会、CDE等权威机构都有相应的指导原则,虽然内容各有不同,但总的思路和原则其实是一致的。指导原则写的是一些很宽泛的指南性的内容,很少涉及具体操作以及为什么要这么做。笔者撰写本文的目的就是根据自己的经验和理解,深入剖析每个验证概念的含义,详细说明方法验证应该怎么做,为什么要这么做,以此为新进入药学研究领域的同仁解决所以然的问题。目标定这么大,而能力又实在有限,不当之处在所难免,敬请大家指正。查看全文
发布时间:2018-06-13 13:26:12 -
【第十季群友会专题】湿法制粒终点控制简介
摘要:本文来自第十季群友会学术交流内容,作者李友峰医药信息新药开发群群友,医药行业就职12年,主要从事面对法规市场的新药以及仿制药研发注册包括仿制药一致性评价。也是一致性评价公众号的主编和持有人。查看全文
发布时间:2018-06-13 12:48:24 -
【经典分享】华海药业质量老大的数据完整性和可靠性问题
摘要:编者分享数据完整性/可靠性法规基本要求、FDA关注的数据完整性7大问题、公司数据完成性/可靠性管理措施、案例讨论等对数据完成性/可靠性进行了系统阐述。查看全文
发布时间:2018-06-13 11:22:28 -
30位专家学者的分享盛宴:USP, AAP和FIP对纳米制剂的发展研讨
摘要:纳米制剂目前还没有一个统一的定义(全球监管机构)。纳米级是指在1-1000nm之间的范围,产品可能因为其粒径,形状或者表面活性而被定义为纳米产品,有时也可能因为产品的目的或功能而被归纳为纳米产品。当前一些多功能小组正在努力制定全球范围内的科学监管指导原则,其中包括CDER的纳米技术指导原则,USP的纳米技术小组委员会,ASTM的E56 纳米技术委员会,ISO的TC200纳米技术,EMA的纳米药物“反射纸”,FDA的纳米技术特别小组标准委员会。查看全文
发布时间:2018-06-13 11:11:30 -
仿制药注射剂稳定性试验方案
摘要:本文详细介绍了仿制药注射剂稳定性试验方案的设计依据,试验样品、放样方案、记录模板,数据评价等细节。查看全文
发布时间:2018-06-13 11:02:06